病理诊断的智能化之路
据世界卫生组织(WHO)统计,恶性肿瘤是全球第二大死因,每年导致近千万人死亡。恶性肿瘤的确诊需要足够充分的证据,组织病理学诊断为最高级别、最可靠的肿瘤诊断方法,是癌症确诊和治疗的基本依据。病理医生的诊断,被视为病情的终极判断。
病理学是医学诊断的金标准,病理报告对于临床医生进一步进行疾病的诊治具有至关重要的作用。我国目前大约只有 1 万多名职业病理医师,按照原卫生部31号文件的规定,每百张床至少要一到两名病理医师,按照这个标准来计算,我国病理医生的缺口至少在 5 - 6 万人左右。病理医生较长的培养周期和人才的缺口,导致了超负荷工作。
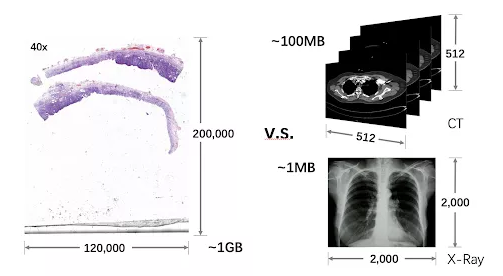
传统病理科使用显微镜对实体切片进行观察,得到诊断报告。随着数字病理的发展,越来越多的切片被数字化,计算机辅助诊断成为可能。不同于 CT、X 光等放射影像,病理影像的体积通常都在 500 MB 至 1 GB,并且信息量大,对深度学习模型的构建和分布式计算系统的架构均提出了很高的挑战。基于 TensorFlow 生态系统的人工智能病理辅助诊断系统 ThoroughInsights,为病理行业带来了突破性创新。
人工智能病理辅助诊断系统
数据、算法、系统,构成了人工智能产品研发的三驾马车。
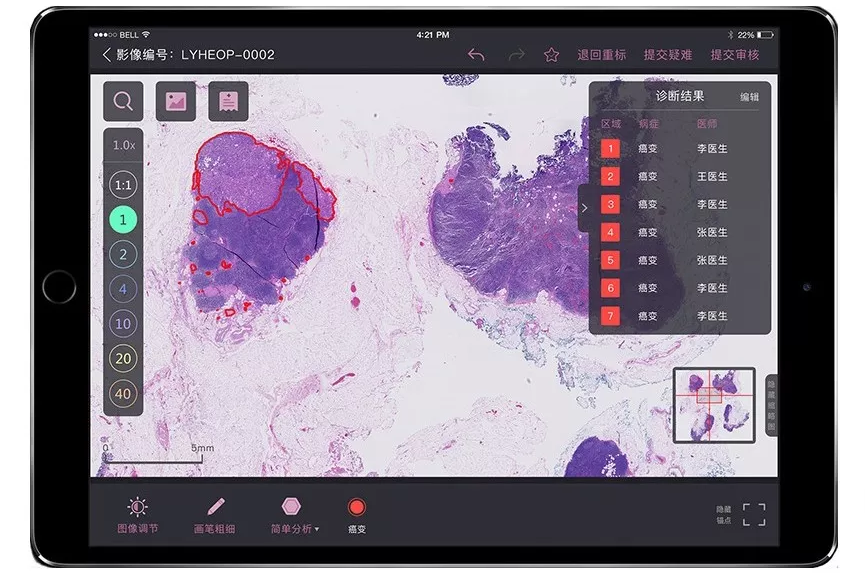
数据是智能的重要入口,我们与顶级三甲医院 40 余名 10 年资以上病理医生合作,通过自研基于 iPad 与 Apple Pencil 的标注工具 ThoroughWisdom,采集了数千张高精度标注的数字病理切片,涵盖了消化与呼吸系统的多个器官。以胃部模型为例,经过切分,训练图像数超过 5000 万,是目前行业内最大的病理高质量像素级标注数据集。
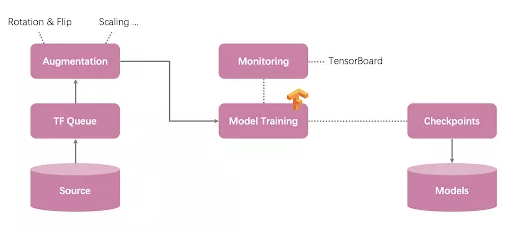
有了训练数据,接下来便是深度学习模型的建立。我们在产品的研发过程中,历经了基于已有模型定制、自研模型、自动化机器学习(AutoML)三个阶段,模型的准确率与泛化能力逐步提高。基于 TensorFlow,我们建立了完整的深度学习流水线,在 10 个 GPU 卡的深度学习集群上,当训练数据达到 5000 万的规模时,在半周内便可以完成一次模型迭代。根据近万张胃部数字病理切片的测试结果,ThoroughInsights 中的胃部癌变识别模型能够达到 100% 的切片级敏感度和超过 85% 的特异性。

模型训练完成后,我们基于 TensorFlow Serving 搭建了一套分布式微服务推理架构,系统具有高可用性和高可推展性,能够将预测任务分配到集群中的所有 GPU 进行并行计算,大幅提高数字病理切片预测的速度。
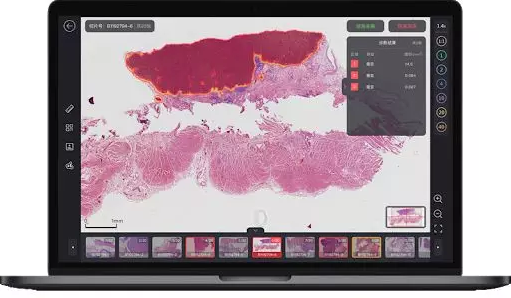
前沿技术在病理领域的落地
目前,胃肠部人工智能病理辅助诊断系统已经在 5 家大型三甲医院落地运行,是全球首个大规模部署的组织病理辅助诊断系统。
病理医生在诊断过程中,不仅可以通过显示器进行疾病诊断,而且能够同时参考计算机的辅助分析结果。人工智能辅助诊断系统具有不知疲倦、客观准确、运算高效等优势,能够帮助医生筛选出大量的阴性病例,从而大幅减轻病理医生的工作负荷。
病理医生可以把一些重复、繁锁的病理诊断工作交由辅助诊断系统完成,比如胃肠镜病理。从而让病理医生有更多的时间进行复杂疾病的诊治和前沿领域的研究,推动医疗技术的发展。
